Estrazione
in Fase Solida (SPE)
L’estrazione
per adsorbimento è un processo fisico tra una fase
solida e una fase liquida in cui la fase solida ha una affinità
maggiore per il composto da isolare rispetto al solvente
in cui lo stesso composto è sciolto. Quando il campione
passa attraverso la fase solida gli analiti vengono concentrati
sulla superficie del materiale adsorbente mentre gli altri
composti presenti nel campione eluiscono senza interagire.
Il risultato è la purificazione e la concentrazione
delle sostanze isolate dal materiale adsorbente. Ciò
può essere ottenuto grazie ad interazioni specifiche
tra i gruppi funzionali dei composti e il substrato della
fase solida.
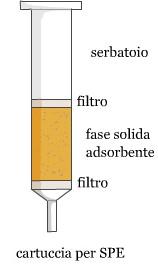  La fase solida adsorbente viene impaccata in una cartuccia.
Il campione viene fatto passare attraverso la cartuccia
in modo che i diversi composti in esso presenti possano
interagire con la superficie adsorbente venendo trattenuti
o meno a seconda della loro capacità di stabilire
interazioni.
La fase solida adsorbente viene impaccata in una cartuccia.
Il campione viene fatto passare attraverso la cartuccia
in modo che i diversi composti in esso presenti possano
interagire con la superficie adsorbente venendo trattenuti
o meno a seconda della loro capacità di stabilire
interazioni.
Si
ha ritenzione quando la fase solida riesce ad immobilizzare
alcuni dei composti presenti nel campione; la ritenzione
cambia in funzione del tipo di adsorbente o del solvente
utilizzato.
#Eluizione
è il processo di rimozione delle sostanze isolate
dall’adsorbente mediante il passaggio nella cartuccia
di un opportuno solvente (da usare nel minor volume possibile).
Maggiore è l’interazione tra adsorbente e analita,
minore è il rischio che questo venga eliminato dalla
cartuccia durante le fasi di lavaggio utilizzate per eliminare
molecole interferenti coadsorbite.
Unità
di misura per caratterizzare ritenzione ed eluizione è
la quantità di solvente necessario per riempire gli
interstizi tra particelle di adsorbente e tutti i pori presenti
nella fase stazionaria della cartuccia di estrazione (bed
volume).
Adsorbenti di 40 µm
con pori di circa 60 Angstroms hanno un “bed volume”
di circa 120 µl
per 100 mg di adsorbente.
La ritenzione è considerata sufficientemente forte
quando possono passare 20 bed volumes di solvente di lavaggio
senza determinare l’eluizione degli analiti isolati.
Una eluizione ottimale richiede non più di 5 bed
volumes di solvente di estrazione.
Il flusso del campione attraverso la cartuccia durante la
fase di estrazione non deve essere superiore ai 5-10 mL/min
per 100 mg di adsorbente
#Capacità
dell’adsorbente è la quantità di analita
trattenuta da una determinata quantità di adsorbente
in condizioni ottimali; varia in funzione degli adsorbenti.
Adsorbenti a scambio ionico hanno capacità di 0,5-1,5
meq/g. Per altri adsorbenti la capacità varia tra
l’1 e il 5% della massa dell’adsorbente (es.
100 mg di adsorbente trattengono fino a 5 mg di analiti).
#Selettività
è la capacità dell’adsorbente di distinguere
tra sostanze da isolare e interferenti da allontanare. Dipende
dalla struttura chimica dell’analita da isolare, dalle
proprietà dell’adsorbente e dalla composizione
della matrice del campione.
La selettività è massima quando l’adsorbente
interagisce solo con i gruppi funzionali dell’analita,
assenti negli altri componenti della matrice del campione.
#Solvatazione
[interazione tra gli ioni di un soluto e le molecole
del solvente, possibile solo con solventi polari (es. NaCl
in acqua, gli ioni Na+ attirano le molecole di H2O)].
La
solvatazione dell’adsorbente è necessaria prima
che questo interagisca con le sostanze da isolare, l’adsorbente
viene bagnato mediante il passaggio di diversi volumi di
un solvente come il metanolo (ma anche acetonitrile, isopropanolo
o THF), che viene a sua volta allontanato (anche se non
completamente) mediante passaggio del solvente che prepara
l’adsorbente al passaggio del campione. Una volta
avvenuta la solvatazione, l’adsorbente non deve essere
lasciato essiccare (bastano 30 secondi di contatto con l’aria
perché l’adsorbente si asciughi).
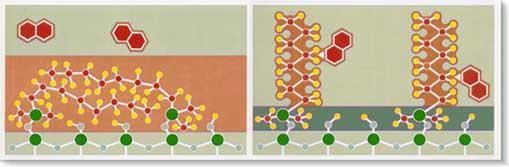
La solvatazione dell'adsorbente rende possibile
il riconoscimento degli analiti
 Adsorbenti Silicei
Adsorbenti Silicei
Sono tra gli adsorbenti più utilizzati, prodotti
mediante reazione tra organosilani e silicati attivi (legame
silil-etere). Stabili a pH variabile tra 2 e 7,5 (sopra
pH 7,5 tendono a sciogliersi in soluzione acquosa; sotto
pH 2 il legame silil-etere diventa labile e i gruppi funzionali
cambiano le loro caratteristiche di specificità)
e con tutti i solventi organici.
Sono materiali rigidi, non si gonfiano in presenza del solvente
come accade per le resine di polistirene. Ciò permette
l’uso successivo di diversi solventi, rendendo possibile
estrazioni anche molto complesse.
 La
fase solida è costituita da particelle di dimensioni
variabili tra i 15 e i 100 µm,
di forma irregolare o sferica, permette un flusso rapido
del solvente in condizioni di vuoto minimo. La
fase solida è costituita da particelle di dimensioni
variabili tra i 15 e i 100 µm,
di forma irregolare o sferica, permette un flusso rapido
del solvente in condizioni di vuoto minimo.
La porosità degli adsorbenti è di circa 60
Angstroms, adeguata a composti con peso molecolare attorno
a 15.000. Molecole di dimensioni maggiori sono escluse dai
pori e non vengono trattenute.
Le proprietà di ritenzione degli adsorbenti silicei
sono dovute soprattutto ai gruppi funzionali legati al substrato
di silice, alla polarità del substrato e ai silanoli
rimasti liberi sulla sua superficie. Interazioni secondarie
tra substrato e analita sono in funzione della polarità
che permette o meno la formazioni di legami idrogeno tra
i silanoli e i gruppi amminici o i gruppi -OH degli analiti
in presenza di un solvente non-polare.
In condizioni acquose i gruppi silanoli producono delle
interazioni ioniche con eventuali gruppi ionici degli analiti
(es. con ammine protonate).
 Interazioni Non-polari
Interazioni Non-polari
Le interazioni non polari più importanti che possono
intercorrere tra fase adsorbente e analita, sono le forze
di Van der Waals (interazioni tra i gruppi C-H di analita
e adsorbente).
C18 (Octadecil-silano) è l’adsorbente
più usato per le interazioni non-polari, non è
selettivo e permette di trattenere molti composti non polari.
Utilizzato per isolare composti anche molto diversi soprattutto
in analisi che necessitano l’estrazione del maggior
numero di composti presenti all’interno di una matrice
(es. analisi ambientali).
Le interazioni non-polari e la ritenzione sono facilitate
in presenza di solventi molto polari (come l’acqua).
In presenza di questo tipo di solventi anche molecole che
presentano gruppi funzionali polari ma che hanno una struttura
non polare possono interagire con l’adsorbente non-polare.
Solventi non-polari invece interferiscono con i meccanismi
di ritenzione.
L’eluizione degli analiti isolati deve avvenire tramite
un solvente non-polare, in grado di rompere le interazioni
non-polari tra analita ed adsorbente.
 Caratteristiche degli analiti: composti con catena achilica,
aromatica, aliciclica o altri gruppi funzionali con una
struttura idrocarburica significativa.
Caratteristiche degli analiti: composti con catena achilica,
aromatica, aliciclica o altri gruppi funzionali con una
struttura idrocarburica significativa.
 Interazioni Polari
Interazioni Polari
Interazioni polari come i legami idrogeno, forze dipolo/dipolo
e molte altre che determinano la distribuzione degli elettroni
tra gli atomi presenti nei gruppi funzionali producendo
una una distribuzione polare delle cariche (+) e (-).
Molecole con gruppi funzionali polari (-OH, -NH2,
C=O, anelli aromatici, gruppi sulfidrili, doppi legami e
gruppi che contengono eteroatomi come O, N, S, P) interagiscono
con i gruppi funzionali polari di opportuni adsorbenti.
Il legame idrogeno è una interazione polare che interviene
tra un gruppo che ha un H legato ad un atomo elettronegativo
(come l’O oppure l’N) e un altro gruppo con
un atomo elettronegativo.
–OH ed –NH2 sono i principali
donatori di legami idrogeno in grado di interagire con gruppi
funzionali che contengono O, N e S.
Interazioni
polari sono tipiche degli adsorbenti silicati (ammine e
gruppi ossidrili sono i gruppi funzionali più sensibili).
La ritenzione è facilitata in presenza di un solvente
non-polare, l’eluizione viene eseguita con solventi
polari in grado di rompere le interazioni polari tra adsorbente
ed analita.
 Caratteristiche degli analiti: molecole contenenti gruppi
funzionali con dipoli, inclusi gruppi con etero-atomi o
gruppi con proprietà di risonanza come anelli aromatici.
Caratteristiche degli analiti: molecole contenenti gruppi
funzionali con dipoli, inclusi gruppi con etero-atomi o
gruppi con proprietà di risonanza come anelli aromatici.
 Interazioni Ioniche
Interazioni Ioniche
Interazioni di scambio ionico tra analiti con gruppi carchi
(+) o (-) e gruppi funzionali dell’adsorbente di segno
opposto.
- Gruppi cationici (+) ammine (I, II, III, IV), ioni Ca2+,
Na+, Mg2+
- Gruppi anionici (-) gr.carbossilici, -SO2OH,
fosfati, sali dell’acido fosforico
Perché avvenga la ritenzione, il solvente deve avere
un pH che permetta sia all’analita sia ai gruppi funzionali
dell’adsorbente di essere carichi, non deve avere
specie ioniche con la stessa carica dell’analita.
E’ necessario conoscere la pKa di ogni gruppo.
(pKa= il pH al quale metà delle molecole in soluzione
sono cariche).
 La matrice del campione
La matrice del campione
Nel
campione, oltre alle sostanze da isolare sono presenti molti
altri composti. L'insieme di queste sostanze costituisce
la matrice.
Lo sviluppo di un metodo di estrazione efficace deve dunque
tener conto sia delle caratteristiche della matrice sia
di quelle del composto da isolare.
Le proprietà dell’analita condizionano la scelta
del tipo di adsorbente e del solvente necessario all’eluizione,
ma si deve tener conto anche delle interazioni tra matrice
ed adsorbente, perché alcuni composti sono in grado
di competere con i siti di interazione per gli analiti,
riducendone di fatto la ritenzione.
Si deve valutare il pH, il carattere polare o non polare,
la forza ionica delle specie presenti, ma anche l’eventuale
adsorbimento dell’analita da parte del sedimento o
il legame con proteine.
Per ovviare all’adsorbimento da parte del sedimento
si può procedere all’ estrazione mediante soxhlet.
Quando l’analita è legato ad una proteina i
sui siti attivi non sono più disponibili e le dimensioni
delle proteine ne escludono la ritenzione da parte dei normali
adsorbenti. Per separare l’analita dalla proteina
si può cambiare il pH del campione (spesso la variazione
del pH modifica le caratteristiche delle proteine), aggiungere
agenti in grado di denaturare la proteina (urea, o reagenti
organici come metanolo o acido formico), far precipitare
le proteine aggiungendo acetonitrile (o acido sulfosalicilico,
ac.tricloroacetico, ac.perclorico).
Se
nella matrice vi è un’elevata concentrazione
di sali è preferibile un estrazione non-polare.
Rimuovere selettivamente i più importanti interferenti
presenti nella matrice impiegando anche diverse tecniche
di estrazione una di seguito all’altra.
 Sviluppo del metodo
Sviluppo del metodo
Sono
due gli approcci alle tecniche di estrazione:
- ritenzione degli analiti da isolare mediante eluizione
selettiva degli interferenti (+ usata)
- ritenzione degli interferenti da parte dell’adsorbente
ed eluizione diretta degli analiti
Per
lo svilppo di un metodo di Estrazione sono necessari:
1.
Valutazione delle caratteristiche dell’analita e dei
composti presenti nella matrice del campione.
2. Scelta dell’adsorbente
3. Testare l’adsorbente per valutare efficienza, selettività,
tipo di eluizione.
4. Verifica del metodo di estrazione su campione reale.
1.
Valutazione delle caratteristiche dell’analita e dei
composti presenti nella matrice del campione
a) scopo del metodo.
- Quale livello di purezza è richiesto per l’analita?
Se l’analisi del campione viene condotta con metodi
molto selettivi come analisi in GC/MS, l’estrazione
può limitarsi ad una semplice ripulitura del campione
dai maggiori interferenti presenti nella matrice; se l’analisi
finale è meno selettiva, la procedura di estrazione
deve necessariamente essere più specifica.
- Quale concentrazione finale è richiesta per l’analita?
La quantità di solvente necessario all’eluizione
dell’analita varia in funzione della quantità
di adsorbente utilizzato e del tipo di estrazione. Maggiore
è la quantità di analita atteso, maggiore
deve essere la quantità di adsorbente necessario
per la sua ritenzione.
- Qual è la composizione dell’isolato?
Per isolato si intende il complesso delle sostanze ritenute
dall’adsorbente, tra queste ci possono essere sostanze
anche molto diverse tra di loro.
b) valutazione dell’isolato.
Struttura delle molecole presenti nell’isolato (presenza
di O, N, P, S). Presenza di gruppi polari e loro eventuale
dislocazione nella molecola. Presenza di ammine o gruppi
ossidrili. Presenza di gruppi ionizzabili, eventuale carica,
pKa. In quali solventi sono solubili. Valutazione degli
effetti del pH sulla solubilità e sulla stabilità
delle molecole. Valutare se le molecole sono libere in soluzione
nella matrice.
c)
valutazione della matrice.
Stato fisico (liquido, gas o solido). Valutare se è
prevalentemente acquosa, non-polare o è un solvente
organico. Trattamento prima dell’analisi (eventuali
diluizioni o altri pretrattamenti). Presenza di composti
interferenti (grassi, proteine) e grado di somiglianza con
l’analita da isolare.
2. Scelta dell’adsorbente
Se l’analita ha regioni della molecola che contengono
solo legami C-H, catene alchiliche, anelli aliciclici, aromatici
o gruppi insaturi può essere ritenuto mediante interazioni
non-polari.
Se l’analita presenta atomi con una forte attività
polare si devono usare interazioni polari.
La presenza di ammine o gruppi –OH permette la formazione
di legami idrogeno.
Si deve valutare la solubilità dell’analita
sia per valutare qual è il solvente migliore per
la sua eluizione, sia per rimuovere gli interferenti senza
eluire l’analita.
Analiti NON-polari sono solubili solo in solventi non-polari
come l’esano, ma questo potrebbe rendere difficile
l’eluizione da un adsorbente non-polare. Valutare
la solubilità al variare del pH o la tendenza al
legame con proteine nei campioni biologici.
Possibili
interferenti presenti nella matrice:
- in estrazioni non polari la presenza di sostanza grasse
che possono essere adsorbite limita il fattore di ritenzione
per l’analita;
- in estrazioni per scambio ionico la presenza di specie
ioniche (Sali);
- la presenza di specie polari in estrazioni polari;
- tensioattivi;
- proteine in grado di interagire con l’analita da
isolare.
3. Testare l’adsorbente
a) Ottimizzare la ritenzione degli standard.
Per preparare gli adsorbenti si fa passare attraverso la
cartuccia prima un solvente di solvatazione adeguato (1
o 2 volte il volume della colonna) in modo da attivare l’adsorbente,
poi un secondo lavaggio per eliminare il solvatante.
Per una estrazione non-polare si eluisce con 10-20 volumi
della stessa soluzione in cui è sciolto lo standard
(miscela acquosa o acquoso/organica); per una estrazione
polare si eluisce con la stessa quantità dello stesso
solvente organico in cui è sciolto lo standard; per
una estrazione per scambio ionico occorre equilibrare l’adsorbente
in modo da raggiungere il pH desiderato.
Se le cartucce sono state esposte all’aria si può
introdurre anche un prelavaggio con il solvente che verrà
utilizzato per l’eluizione degli analiti, in modo
da allontanare eventuali contaminanti.
Se si usa silice come adsorbente, il prelavaggio non è
necessario.
Una volta attivata la cartuccia non si deve lasciarla asciugare.
b)
Ottimizzare l’eluizione degli standard (cioè
trovare il solvente che eluisce l’isolato con il minor
volume possibile) ed identificare i solventi per il lavaggio
(cioè quei solventi che non eluiscono l’analita,
ma che permettono di eliminare gli interferenti presenti
nella matrice).
- solventi di eluizione. Testare diversi solventi, raccogliere
l’eluato e scegliere solo quei solventi che permettono
un recupero superiore al 90%
- solventi di lavaggio. Testare diversi solventi (con polarità
opposta a quella dell’analita), raccogliere l’eluato
e scegliere quello che rimuove la maggior parte della matrice
senza eluire l’analita.
c) Testare la matrice.
d)
Testare l’adsorbente. Scegliere tra un set di adsorbenti
con polarità differenti quello più adatto
per la ritenzione dell’analita.
Fonti
- Sorbent Extraction Technology di D.D.Blevins,
M.F.Burke, e altri; edited by N.Simpson e K.C.Van Horne
- Varian
|