CINETICA DI COMBUSTIONEPrerequisiti.La combustione è una complessa reazione che segue un meccanismo radicalico, nel complesso è però analizzabile come una qualsiasi altra reazione e molto utile per osservare due tipi base di cinetica: la caduta esponenziale e la velocità costante.Vedasi al riguardo le pagine relative alla cinetica I in questo stesso sito i grafici delle prime due righe ivi descritti in maneira teorica. Attrezzatura e Strumenti.In laboratorio saranno presenti:
ProcedimentoSi ritaglia un pezzo di carta da filtro di almeno un grammo e si accartoccia in modo da inserirlo in una capsula di porcellana.Si determina alla bilancia la massa della carta al netto della capsula. Rimanendo sulla bilancia si accende la carta e contemporaneamente si fa partire il cronometro per misurare i tempi. E' necessario monitorare la combustione almeno ogni dieci secondi per avere dei buoni dati iniziali con cui procedere per realizzare due grafici: 1) della massa contro il tempo e 2) della variazine di massa rispetto all'intervallo di tempo. Si segue la compustione fino a completamente, per un grammo di carta da filtro sono sufficienti due minuti. I cellulari permettono di fare brevi riprese video (al display della bilancia) che permettono una maggiore precisione nella trascrizione dei dati. OsservazioniLa reazione di combustionse si scrive facilmente bilanciando la reazione con la formula della cellulosa.[C6H10O5]n (s) + 6n O2 (g) —» 6n CO2 (g) + 5n H2O (g)
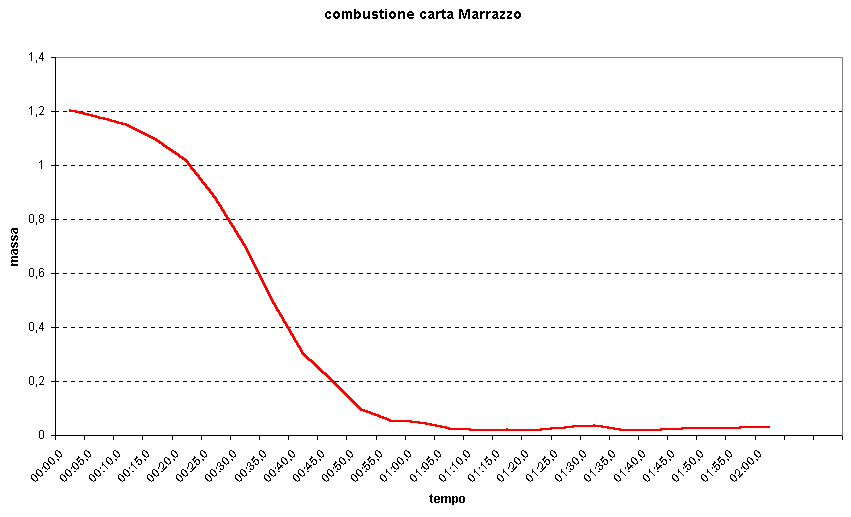
pericoli e precauzioniParticolare cura si deve prestare quando si misurano le masse tenuto conto anche della sensibilità effettiva della bilancia, infatti movimenti nell'aria circostante interferiscono pesantemente sui valori misurati.L'uso della carta da filtro, cellulosa praticamente pura, evita che il laboratorio si appesti di odore di bruciato, comune con altri tipi di carta. RisultatiDalla tabella dati seguente:
In generale si possono ottenere grafici più o meno irregolari.
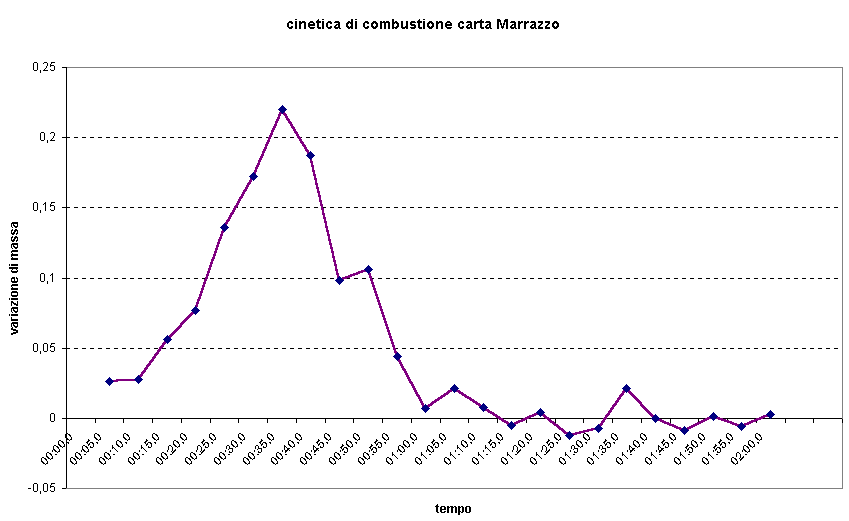
Se mettiamo in grafico la variazione di massa in funzione del tempo otteniamo infatto un grafico
abbastanza irregolare ma comunque significativo.
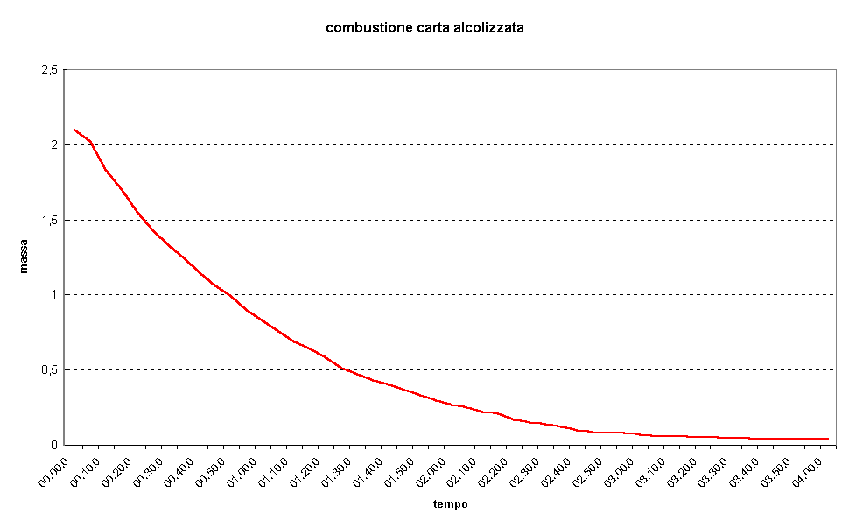
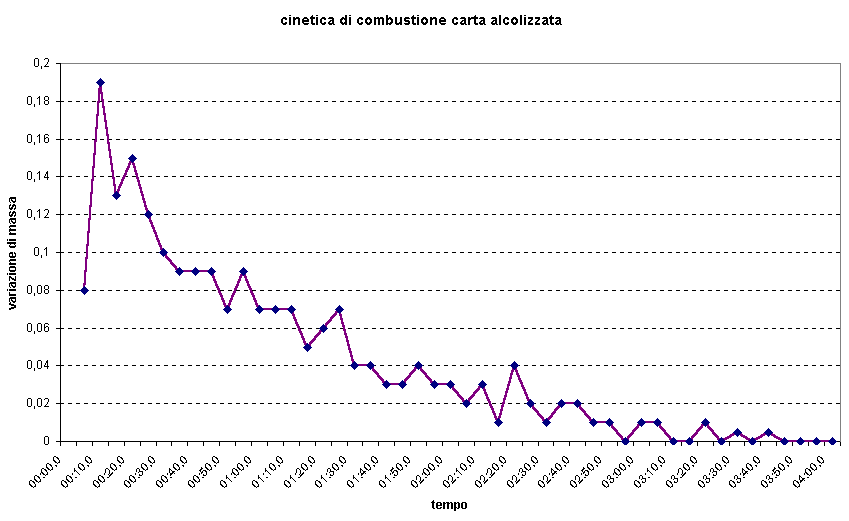
Il risultato migliore si ha con carta "alcoolizzata" dove quindi la fase iniziale di assestamento
della combustine è molto rapida.
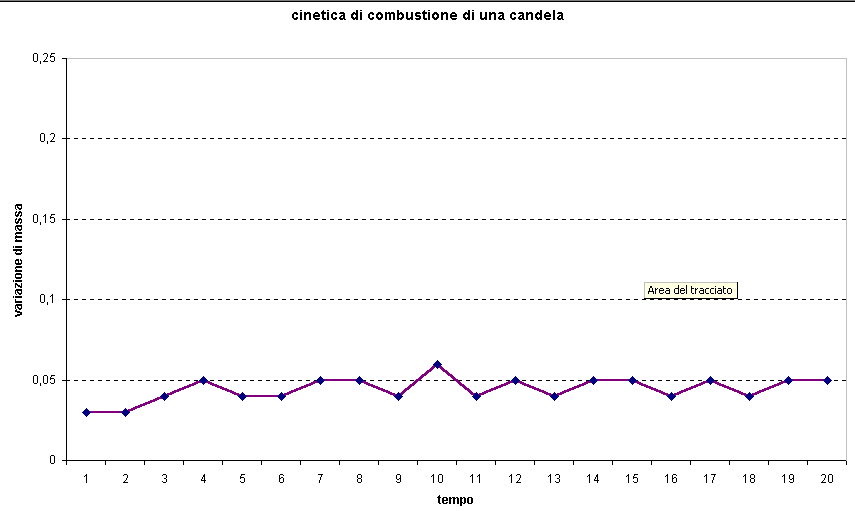
Operando con una candela si ha invece una combustione molto regolare indice di una velocità
costante come si può vedere dai seguenti due grafici. ConclusioniLa prova è stata portata a termine con successo nei termini previsti dal tempo a disposizione (circa 50 minuti).Infatti la combustione richiede due - tre minuti ed il resto del tempo si è utilizzato per la realizzazione del grafico, pulire e lavare le capsule. RingraziamentiI dati di origine ed i primi due grafici sono stati ottenuti dallo studente Marrazzo Luca (a.s. 2014/2015).Si ringraziano anche tutti i ragazzi che hanno eseguito l'esercitazione e la prof.ssa Anna Maria Zampiga.
|