|
TECNOLOGIE DI PRODUZIONE
Una delle
caratteristiche dell’idrogeno è di essere prodotto da
molte fonti quali l’acqua, i combustibili fossili e le
biomasse, sfruttando diverse tecnologie tra cui le
principali sono:
◊Elettrolisi dell’acqua
◊Steam reforming del gas
naturale
◊Ossidazione parziale non
catalitica d’idrocarburi pesanti
◊Gassificazione del
carbone
◊Gassificazione e pirolisi
delle biomasse
► Elettrolisi
dell’acqua
Il metodo più semplice per la produzione dell’idrogeno
è costituito dal processo d’elettrolisi.
Esso consiste in una reazione d’ossidoriduzione non
spontanea che avviene, all’interno di una cella
elettrolitica, a spese d’energia elettrica fornita
dall’esterno attraverso una batteria o un generatore
di corrente continua.
La figura (1.2) mostra lo schema semplificato di una
cella elettrolitica.
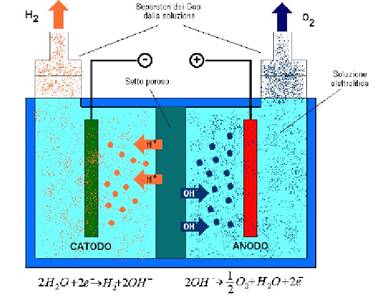
La cella è
costituita da un recipiente che contiene:
◊Una soluzione ionica
acida o alcalina
◊Un setto poroso che
consente il passaggio degli ioni e ne impedisce il
mescolamento dell’ossigeno con l’idrogeno
◊Una coppia d’elettrodi,
generalmente realizzati in platino.
Quando agli elettrodi viene applicata una d.d.p.
opportuna, sulla loro superficie hanno inizio le due
semireazioni, di riduzione (al catodo) ed ossidazione
(all’anodo)
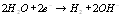 (1.3)
(1.3)
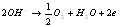 (1.4)
(1.4)
Queste danno luogo alla reazione complessiva:
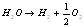 (1.5)
(1.5)
La d.d.p. da applicare agli elettrodi deve essere
superiore alla f.e.m. della pila in cui si facesse
avvenire il processo spontaneo, inverso a quello
d’elettrolisi. (La tensione da applicare in acqua
pura, a 25°C ed 1 atm, è 1.24 V)
L’idrogeno e l’ossigeno, liberati al catodo ed
all’anodo, vengono raccolti ed immagazzinati in
opportuni recipienti pressurizzati. L’idrogeno
ottenuto presenta un elevato grado di purezza.
L’elettrolisi, pur essendo il metodo più comune per la
produzione d’idrogeno, incontra molte difficoltà di
sviluppo. Questo è dovuto soprattutto dal fatto che i
costi del prodotto finale sono molto alti a causa
della limitata quantità d’idrogeno prodotta rispetto
all’energia necessaria per il processo. La figura
(1.6) mostra il bilancio energetico dell’elettrolisi
di un litro d’acqua.
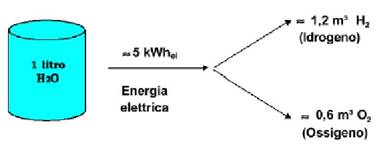
La generazione
d’idrogeno richiede elevate quantità d’energia
elettrica per dissociare le molecole d’acqua a causa
del forte legame chimico tra idrogeno ed ossigeno.
Proprio per questo motivo l’elettrolisi è conveniente
solo in quei paesi dove l’elettricità ha un basso
costo, come in Canada o in Norvegia, oppure quando si
possa sfruttare l’energia prodotta in eccesso da
centrali elettriche tradizionali.
Per risolvere questo problema una possibile via può
essere quella di alimentare il processo di
dissociazione dell’acqua attraverso l’energia
elettrica prodotta da fonti rinnovabili, in
particolare da centrali fotovoltaiche. Ciò consente di
produrre l’idrogeno senza alcun impatto negativo
sull’ambiente ed al tempo stesso svincola il costo del
prodotto da quello dell’energia necessaria a produrlo.
Comunque sia, il costo per la produzione d’idrogeno
attraverso elettrolisi resta il più alto rispetto a
tutte le altre tecnologie. |