
funzionamento di una pila
una barretta di
zinco elettricamente neutra viene immersa in una soluzione
contenente ioni Zn++ (esempio ZnSO4 +
H2O)
spontaneamente alcuni
atomi di zinco passano in soluzione trasformandosi in ioni Zn++
(ossidazione) e rendendo
così negativa la barretta di zinco
si stabilisce un equilibrio dinamico tra tendenza degli atomi a
ossidarsi
passando in soluzione e tendenza degli ioni a ridursi
riacquistando gli elettroni
all'equilibrio la carica
negativa della barretta di zinco avrà un valore che dipende
fondamentalmente dalla tendenza propria dello zinco a ossidarsi
Zn° - 2e
<-------> Zn++

un fenomeno
simile avviene immergendo una barretta neutra di rame in una
soluzione
contenenente ioni di Cu++ (es.CuSO4 + H2O)
all'equilibrio la carica negativa
della barretta di rame avrà un valore che dipende
fondamentalmente dalla tendenza propria del rame a ossidarsi
Cu° - 2e <------> Cu++
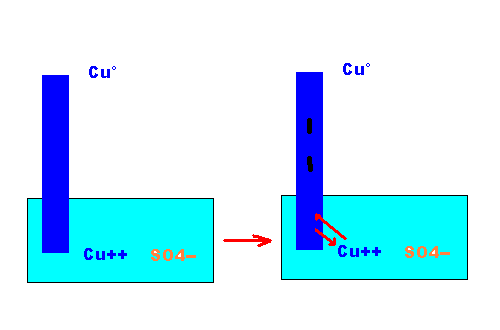
si può notare che lo zinco raggiunge
l'equilibrio dopo aver ossidato un maggior numero di
atomi rispetto al rame,e quindi la carica negativa sulla barretta
di zinco è maggiore di
quella associata alla barretta di rame:si hanno due SEMICELLE
ognuna formata da
ELETTRODO in presenza di una soluzione di suoi IONI
ELETTRODO più negativo = ANODO o polo negativo
ELETTRODO meno negativo = CATODO o polo positivo
collegando opportunamente
le due semicelle si ha una pila