CENNI TEORICI
Tutte le molecole sono capaci di assorbire delle caratteristiche lunghezze d’onda di radiazione elettromagnetica. Quando questo avviene, l’energia della radiazione viene trasferito alla molecola e l’intensità della radiazione diminuisce come conseguenza. Esiste una relazione tra il grado di attenuazione della radiazione e la concentrazione della sostanza che assorbe la radiazione stessa..
Considerando uno strato di spessore b, in cm, di una soluzione di un certa sostanza, attraversato da una determinata radiazione monocromatica, assorbita dalla sostanza stessa, l’intensità della radiazione emergente dalla soluzione avrà un’intensità I minore di quella Io entrante. Il rapporto tra l’intensità emergente e quella entrante nella soluzione è definito trasmittanza (T):
![]()
che può essere espressa anche in percentuale.
Per assorbanza A, invece, si definisce il logaritmo negativo della trasmittanza:
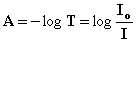
La legge di Lambert Beer stabilisce una proporzionalità diretta tra l’assorbanza e la concentrazione della specie assorbente:
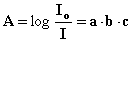
dove a è una costante di proporzionalità, chiamata assorbanza specifica, b è la spessore di soluzione attraversato dalla radiazione, espresso in cm, c la concentrazione della sostanza assorbente nella soluzione. Se quest’ultima è espressa in moli/litro, l’assorbanza specifica prende il nome di coefficiente di estinzione molare, ε:
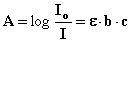
La legge di Lambert-Beer descrive bene il comportamento in assorbimento di soluzioni diluite, cioè con concentrazione generalmente fino a 0,01 M. Al di là di tale limite si osservano delle deviazioni dalla proporzionalità diretta tra assorbanza e concentrazione. Tali deviazioni possono derivare da diverse cause.
1. Innanzitutto ad alte concentrazioni le distanze tra gli ioni o le molecole delle specie assorbenti diminuiscono al punto che ogni particella influisce sulla distribuzione di cariche elettriche delle sue vicine, modificando la loro capacità di assorbire una data lunghezza d’onda di radiazione.
2. Quando le specie chimiche assorbenti subiscono reazioni di dissociazione o di associazione. In questi casi le nuove sostanze prodotte possiedono coefficienti di estinzione molari differenti. Le deviazioni dalla legge di Lambert-Beer dipendono quindi dai valori delle costanti di equilibrio di tali reazioni e dai valori dei coefficienti di estinzione molare. Esse vengono indicate come deviazioni chimiche.
3. La legge di Lambert-Beer si applica solo a misure in luce monocromatica. Nel caso reale degli strumenti usati nella spettroscopia, gli spettrofotometri, non è possibile utilizzare sorgenti realmente monocromatiche. Infatti ogni spettrofotometro è generalmente dotato di una sorgente continua policromatica alla quale viene abbinato un filtro o un reticolo monocromatore che permette di selezionare una banda di lunghezze d’onda più o meno simmetrica intorno alla lunghezza d’onda che deve essere usata.. Si verificano allora delle deviazioni dalla legge di Lambert-Beer, che vengono definite deviazioni strumentali, le quali possono essere attenuate con particolari accorgimenti.