CALCOLO DEL PUNTO ISOELETTRICO DEGLI
AMINOACIDI
Gli aminoacidi sono molecole a
carattere anfotero. Gli anfoteri sono composti che possono comportarsi come
acidi o come basi, a seconda delle situazioni che si verificano in soluzione:
Ka1
Ki=Kw/Ka2
H3O+ + NH2―
RCH―COO- ←
+NH3―
RCH―COO- + H2O →
+NH3―
RCH―COOH +
Dove
Ka1 e Ka2 sono rispettivamente le costanti di
equilibrio di dissociazione acida dei gruppi ammonio (+NH3) e carbossilico (COOH)
Potendo
dissociarsi in entrambi i modi, deve esistere un valore di pH a causa del quale
la dissociazione in entrambe le direzioni è quantitativamente la stessa. Ciò
corrisponde al verificarsi della seguente uguaglianza:
[NH2― RCH―COO-] = [+NH3―
RCH―COOH] (1)
Scrivendo le espressioni
delle costanti di acidità, di basicità e del prodotto ionico dell’acqua,
relative cioè ai tre equilibri simultanei che si verificano nella soluzione
dell’anfolita e considerando l’eguaglianza (1), si ottiene:

![]()
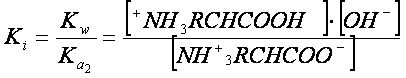
![]()
Dividendo Ka per Ki e imponendo la condizione (1) si ha:
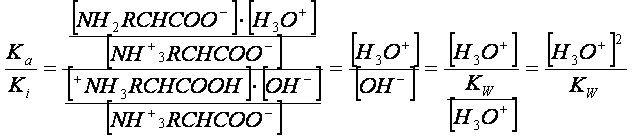
ma, essendo Ki=Kw/Ka2,
si ottiene:
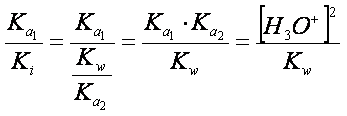
Da cui:
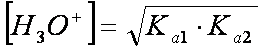
Torna a 20-AMMINOACIDI.htm