Torna a ARGOMENTI DI CHIMICA ORGANICA
LIPIDI
I lipidi si dividono in diverse classi:
a)
Triacilgliceroli (trigligeridi)
b)
Fosfogliceridi
c)
Sfingolipidi
d)
Glicolipidi
e) Cere
f) Terpeni
a)
Triacilgliceroli (trigligeridi)
Sono
composti naturali, triesteri del glicerolo con acidi carbossilici (detti acidi
grassi) a catena lineare lunga caratterizzata solitamente da 14-20 atomi di
carbonio, comunque sempre con numero pari
di atomi di carbonio. La catena lineare idrocarburica può essere satura o
insatura, con uno o più doppi legami. I trigliceridi che sono liquidi a
temperatura ambiente vengono chiamati oli,
quelli solidi, grassi. I primi, insaturi, presentano doppi legami in
una o più catene idrocarburiche, i secondi, saturi, hanno solo legami semplici.
La
formula generale dei trigliceridi è:
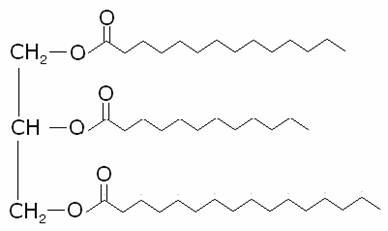
La
tabella riporta alcuni dei più comuni acidi grassi:

I saponi sono i prodotti della reazione di idrolisi
alcalina dei trigliceridi (chiamata anche reazione di saponificazione):
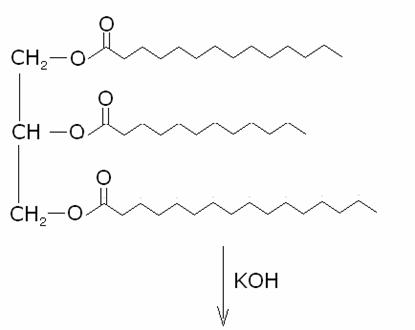
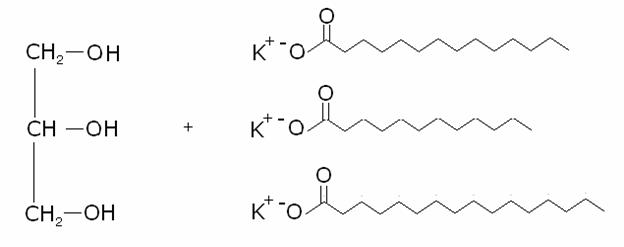
I
Sali degli acidi grassi sono poco solubili in acqua a causa della lunga catena
idrocarburica: essi formano piuttosto delle micelle, cioè degli aggregati sferoidali in cui le catene
idrocarburiche, idrofobe, stanno all’interno della micella, che è una zona
idrofoba, mentre l’estremità polare idrofila, costituita dal gruppo
carbossilico, è orientata verso l’esterno ed è a contatto con l’acqua. Si ha
così uno strato di cariche negative sulla superficie delle singole micelle,
che, invece di aggregarsi, si respingono, rimanendo disperse in acqua. L’azione
detergente dei saponi è dovuta al fatto che lo strato untuoso che generalmente
ricopre lo sporco viene disperso, con un’azione meccanica, in minute goccioline
oleose, che sciolgono la parte idrocarburica delle molecole dei saponi
lasciando all’esterno i gruppi carbossilici carichi negativamente che si
respingono reciprocamente. In tal modo le micelle vengono facilmente asportate dall’acqua:
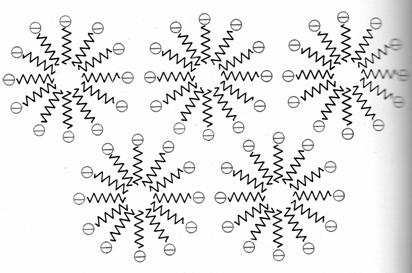
Molti
tipi di molecole sintetiche con
caratteristiche analoghe ai saponi hanno
un’azione detergente. Queste molecole hanno come elemento strutturale una lunga
catena apolare idrofoba e
un’estremità polare idrofila.
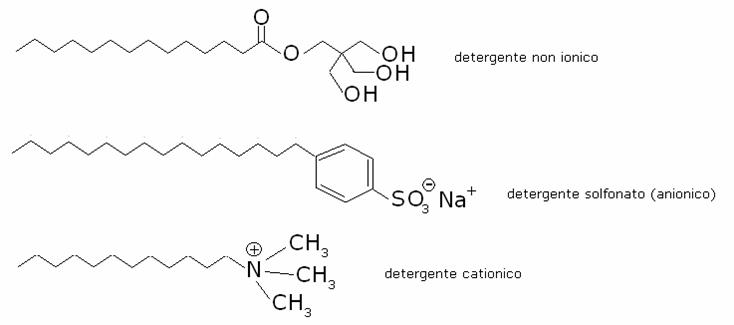
L’estremità polare può essere un gruppo con carica negativa, come nei detergenti
solfonati, un gruppo con carica
positiva come nei detergenti
cationici, o un gruppo neutro ma
ricco di ossidrili come nei saponi
non ionici. Esempi:
b)
fosfogliceridi
Sono
lipidi di primaria importanza, essendo i costituenti delle membrane cellulari.
Differiscono dai trigliceridi per il fatto che solo due ossidrili del glicerolo
(uno legato ad uno dei due atomi di carbonio primari e l’altro a quello
secondario, centrale, del glicerolo)
sono esterificati con acidi grassi, mentre il terzo ossidrile è esterificato
con acido fosforico (per questo tali lipidi vengono anche chiamati acidi fosfatidici). L’acido fosforico,
che è un acido triprotico (ha tre funzioni ossidrili legati all’atomo di
fosforo) è legato a sua volta alla colina,
molecola altamente polare, mediante
esterificazione col suo secondo gruppo
ossidrile. In questo caso si hanno le fosfatidilcoline
o lecitine:
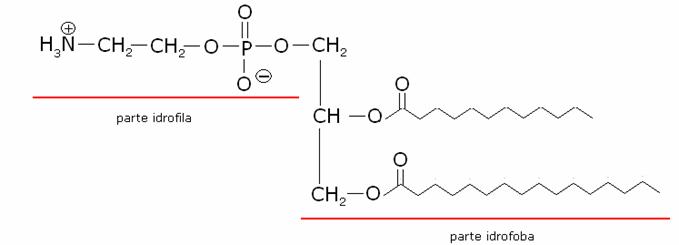
Se
l’acido fosforico è esterificato con l’etanolammina si hanno le fosfatidiletanolammine o
cefaline. Se è esterificato con
c)
Sfingolipidi
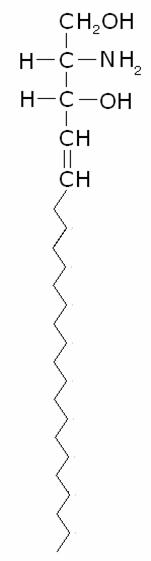
Sono
importanti componenti delle membrane cellulari cerebrali, costituite dalla sfingosina, un amminodiolo a catena
lunga, che esplica la stessa funzione del glicerolo nei trigliceridi e nei
fosfolipidi:
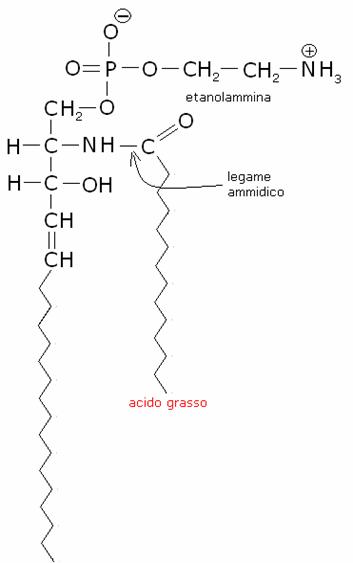
Nelle
sfingomieline il gruppo alcolico
della sfingosina è esterificato da un ossidrile
fosforico legato a etanolammina o a colina. Il gruppo amminico è impegnato in un
legame ammidico con un acido grasso:
Torna a ARGOMENTI DI CHIMICA ORGANICA