Relatrice: La Sala Rachele,
Infermiere Area Critica Cardiologica - U.T.I.C.
Ospedale Maggiore di Parma -
“……….
L’infermiere è responsabile dell’ assistenza infermieristica generale, a
lui compete la identificazione dei problemi/risorse della persona, la
pianificazione degli interventi e la valutazione dei risultati raggiunti
……….” : lo ricorderete sicuramente, è il mandato legislativo del D.M.
739/94 profilo professionale dell’ infermiere; ho voluto citarlo come
introduzione, proprio perché è espressione della conquistata “ AUTONOMIA
” dell’infermiere, un elemento che spicca in maniera particolare nell’
assistenza ad un paziente con STEMI
(ST elevation myocardial infarction)
Scopo di questa relazione è quello di fornire uno strumento operativo che alla luce della continua
evoluzione clinica e tecnologica del trattamento dell’ IMA, possa garantire il
più possibile una assistenza infermieristica qualificata, basata soprattutto
sull’importanza di due elementi:
tutto
questo deve mirare ad un unico obiettivo cioè :
TEMPESTIVITA’ DEGLI INTERVENTI ASSISTENZIALI
poiché
IL
TEMPO E’ MUSCOLO SALVATO.
Il modello assistenziale
comprende due fasi: la prima di accettazione del paziente con
STEMI e la seconda di attuazione della strategia terapeutica.
Come
metodo espositivo ho scelto di descrivere il piano di assistenza di ogni fase
utilizzando il seguente schema:
PRIMA
FASE-
CLINICHE:
- rischio morte/invalidità dovuto all’occlusione
dell’IRA ( vaso coronarico correlato all’IMA );
- dolore toracico;
RELAZIONALI:
-
ansia e paura del paziente dovuta alla non conoscenza di ciò che sta accadendo;
OBIETTIVO:
- Priorità assoluta è portare il paziente in condizioni di ricevere
il trattamento terapeutico;
-
Tranquillizzare ed ottenere la massima collaborazione del paziente;
PERSONE
COINVOLTE:
INTERVENTI:
INFERMIERE
LEADER:
Il flusso di informazioni
sarebbe meglio che venisse registrato su appositi moduli scritti al fine di
stilare una specifica “check list” contenenti dati riguardanti la prima fase
di valutazione del paziente come:
§
inizio
del dolore;
§
terapia
eseguita (che dovrebbe comprendere soprattutto quella con ASPIRINA; è
importante comunque accertarsene e provvedere in caso di non avvenuta
somministrazione);
§
esami
ematici e strumentali eseguiti;
§
eventuali
complicanze durante il trasporto ecc.;
ciò dovrebbe evitare
fraintendimenti e/o omissioni di dati importanti dovuti alla trasmissione orale
delle informazioni;
1.
stimare l’area del miocardio
a rischio durante le prime ore di STEMI in evoluzione; infatti
è emerso da uno sottostudio GISSI I che tanto più è elevato il numero di
derivazioni con sopraslivellamento del segmento ST tanto peggiore è la
prognosi;
E’
da considerare che il sopraslivellamento stabile del tratto ST, è significativo
se è superiore a 0.2 mV ( 2 mm o due quadratini sulla carta millimetrata )
nelle derivazioni V1 V3 e 0,1 mV nelle altre derivazioni;
2.
identificare
la sede dell’IMA.
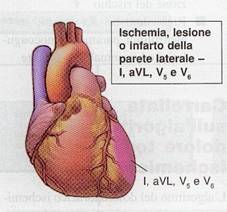
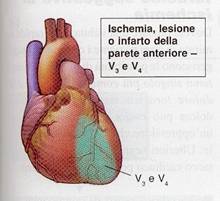
Dalla
seguente figura possiamo notare le correlazioni tra ECG a 12 derivazioni e
anatomia delle arterie correlate:


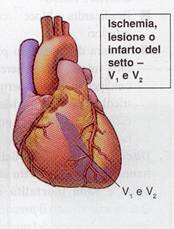
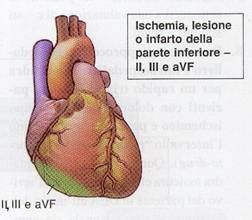
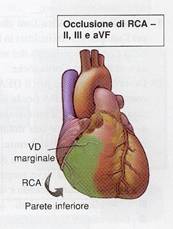
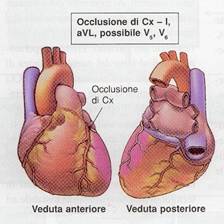
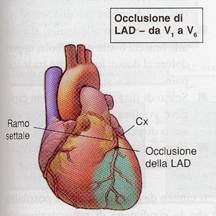
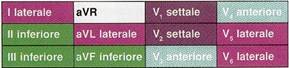
Se
la sede è inferiore si procede anche alle derivazioni destre e posteriori
sinistre per escludere un interessamento della parete posteriore del cuore e del
ventricolo destro.
La
sede ANTERIORE è considerata di più
grave rischio in quanto coinvolge una estesa porzione del ventricolo sinistro.
Raccolta
dati: dinamica del malessere iniziale ( es. dolore toracico insorto durante uno
sforzo fisico ecc.); peso; altezza; eventuali allergie note; recenti interventi
chirurgici; recapito telefonico sempre reperibile in caso di necessità ecc. A
questi dati integrare anche elementi predittori di alto rischio acuto di
mortalità quali:
1.
età avanzata
2.
storia di coronaropatia
(pregresso IMA - BPAC)
3.
diabete
4.
portatore di altre patologie (
ICTUS – IRC )
5.
ipertensione arteriosa ecc.
KILLIP I
IMA che non si accompagna a segni o sintomi di insufficienza
cardiaca;
KILLIP
II IMA con
iniziale insufficienza di pompa testimoniata dalla presenza di rantoli
bibasilari;
KILLIP
III
IMA con EPA
KILLIP
IV IMA con
shock cardiogeno
Le reazioni
che spesso il paziente può manifestare sono:
paura di ciò
che può capitare – senso di morte imminente;
paura di
comunicare;
panico;
ansia, senso
di abbandono e di ambiente ostile
INFERMIERE DI TURNO
vista
l’alta prevalenza di diabete fra i pazienti con cardiopatia ischemica e
l’effetto devastante del diabete sulla prognosi a breve e lungo termine, si è
deciso di adottare lo schema DIGAMI 2 ;. questo schema consiste nel controllo
aggressivo della glicemia con insulina nei pzazienti diabetici o con glicemia
superiore a 198 mg/d l (
secondaria alla stimolazione del sistema adrenergico ) ricoverati entro 24 ore
dall’insorgenza dei sintomi.
A
questo punto termina la prima fase del piano assistenziale che descrive il
quadro clinico del pz e sulla base della quale il medico potrà eseguire una
stratificazione del rischio e la scelta del percorso terapeutico appropriato.
STRATEGIE
TERAPEUTICHE:
§
TROMBOLISI
§
PTCA
PRIMARIA
§
PTCA
DI SALVATAGGIO O RESCUE
§
PTCA
FACILITATA
TROMBOLISI
OBIETTIVO:
§
riperfusione dell’area infartuale con conseguente
ripristino del flusso ematico coronarico TIMI 3 ; cioè un flusso normale e
riperfusione completa.
PERSONE
COINVOLTE:
INTERVENTI:
- Informazione al paziente.
Se
l’informazione è gestita correttamente intrinsecamente diventa un supporto
psicologico capace spesso di ridurre la carica ansiogena ed aumentare quella di
collaborazione. Inoltre, informare il paziente delle possibili sensazioni
sgradevoli che la trombolisi potrebbe provocare, come nausea; vampate di calore;
malessere improvviso; fatica a respirare ecc. aiuta anche l’infermiere a
discernere meglio tra sintomatologia clinica e sensazioni soggettive.
CRITICITA’
CLINICHE:
INTERVENTI:
ematomi,
soluzioni di continuo (escoriazioni, ulcere vascolari, venipunture
ecc.) in modo da identificare i punti potenzialmente a rischio di
sanguinamento.
B Erogazione del trattamento fibrinolitico
TEMPO
PORTA - FARMACO
il
meno possibile.
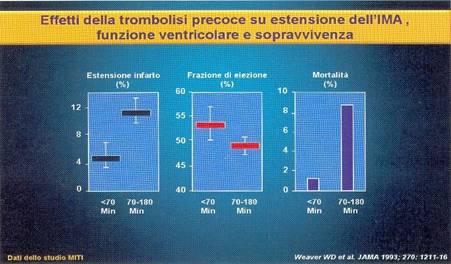
Iinfatti
una TBL effettuata precocemente, è risultata associata ad una minore estensione
dell’area infartuale, ad una migliore funzione del ventricolo sn e ad una
riduzione della mortalità (STUDIO MITI).
INTERVENTI:
Nella
nostra U.O. il fibrinolitico più usato è l’rtPA; per la modalità di
infusione ci serviamo della seguente tabella:

C Preparazione e somministrazione farmaci ulteriori prescritti:
-
EPARINA (UFH) non frazionata : 60U /Kg per un massimo di 4000 Unità in bolo-
12U/Kg/ora per un massimo 1000U/h dose iniziale e poi proseguire secondo il
normogramma:
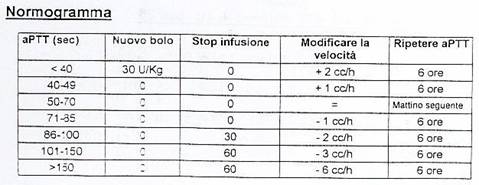
Il
monitoraggio dell’aPTT deve essere fatto a 3, 6, 12, 24 ore dall’inizio del
trattamento; mantenendo un target
tra 50-70, poiché si è visto che entro questi range si ha un minor rischio di
sviluppare complicanze emorragiche cerebrali.
Per
la determinazione in tempo reale dell’aPTT ci serviamo di un dispositivo: il
CaguCheck.
-
NITRODERIVATI : hanno un effetto sul vasospasmo; diminuiscono il
pre e post carico
e la P.A
.
-
BETA BLOCCANTI : diminuiscono il consumo di ossigeno con conseguente
preservazione della funzione ventricolare sinistra e prevengono
l’estensione dell’area infartuata, diminuiscono anche l’attività
adrenergica con conseguente riduzione delle aritmie ventricolari e del rischio
aritmico.
D Controllo
del dolore
INTERVENTI:

E Efficacia terapia riperfusiva
INDICATORI
CLINICI:
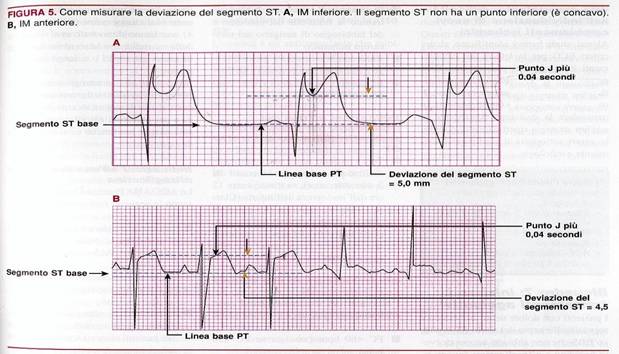
- Misurare a 0,04’ (1 mm) dopo il punto J. Il punto J è il punto di congiunzione (cambiamento dell’angolo) tra il complesso QRS e l’onda ST.
- La linea di riferimento per questa misura è il segmento PR. Una linea tracciata dall’inizio dell’onda P alla fine dell’onda T è più utile e valida, in particolare nei pazienti con ECG che evidenzia segmenti ST concavi o convessi e onde T iperacute.
La risoluzione del segmento ST è completa se
superiore o uguale al 70%; parziale tra i 30-70%; assente se
inferiore 30% a 90 minuti inizio TBL.
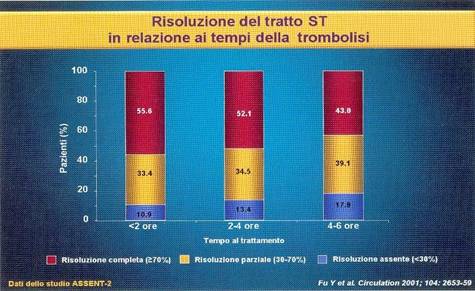
Dati
di un recente studio ASSENT – 2 hanno dimostrato che una più completa
risoluzione del sopraslivellamento del segmento ST, si osserva nei pazienti
sottoposti precocemente a trombolisi:
I
pazienti con IMA, nei quali la terapia riperfusiva risulta efficace, rilasciano
in circolo enzimi e proteine cardiache più velocemente (fenomeno del washout)
dei pazienti con occlusione permanente, per cui tanto migliore è la
riperfusione tanto più precoce dovrebbe essere il picco enzimatico e,
soprattutto tanto migliore dovrebbe essere il ritorno a valori “normali.”.
F Individuazione precoce di complicanze:
INTERVENTI:
§
Rilievo
parametri clinici ( PA FC FR SpO2 )
ogni 10’
§
Osservazione
clinica continua del paziente per rilevare eventuale presenza di orticaria;
broncospasmo ecc. da reazione allergica.
§
Monitorare
cute e mucose per individuare la comparsa di:
Petecchie
Ematomi
Emorragie
congiuntivale
Gengivorragia
Epistassi
§
Monitorare
urine - feci – escreato per individuare la presenza di
Ematuria
Ematemes
Melena
Emoftoe
§
Osservare
stato neurologico del paziente per individuare segni di eventuale emorragie
cerebrali come: alterazione stato di coscienza, alterazioni sensitivo-motorie;
nisocoria ecc.
§
Comparsa
di dolori in sede addominale e/o in sede lombare indicativi di presenza di
ematoma retroperitoneale
§
Tenere
a portata di mano il carrello di emergenza
§
Controllare
la diuresi e il bilancio delle 24
ore
PTCA
PRIMARIA
PRIMA
DELLA PROCEDURA
OBIETTIVO:
·
Riperfusione
dell’area infartuale con conseguente ripristino del flusso ematico coronario
TIMI 3, soprattutto a valle dell’occlusione.
·
intervallo
tra tempo porta e inizio in sala di caterizzazione il più breve possibile.
PERSONE
COINVOLTE:
§
1 unità
infermiere leader
§
1
unità infermiere di turno
§
1unità
OTA
§
1
unità medico
CRITICITA’
RELAZIONALI:
§
ansia e
preoccupazione dovute alla non conoscenza della procedura.
INFERMIERE
LEADER
INTERVENTI:
§
Attivare una
relazione mirata a rassicurare il paziente, informandolo sulla procedura (entro
le proprie competenze) con atteggiamento calmo e rispondendo alle eventuali
domande. Anche la mimica facciale come i movimenti fermi e sicuri durante
l’esecuzione delle varie manovre inf. (BODY LANGUAGE) hanno una certa
importanza nello stabilire un rapporto di fiducia
§
Informarlo
sulle sensazioni sgradevoli che potrebbe provare durante la procedura percutanea
come ad esempio: il fastidio durante l’anestesia locale; il dolore anginoso
durante il gonfiaggio del palloncino in coronaria; sensazione di calore intenso
provocato dal MDC.
§
Spiegargli
l’importanza della sua partecipazione attiva
§
Posizionare
il catetere vescicale solo se vi sono indicazioni o se prescritto dal medico.
§
Far
firmare i consensi per la procedura.
PERSONALE
OTA
§
Esecuzione
tricotomia degli inguini modo pantaloncino poiché di solito è l’accesso
arterioso femorale ad essere reperito.
§
Verificare
che non siano presenti gioielli e altri oggetti personali, e che i capelli siano
completamente raccolti in una cuffia.
INFERMIERE
DI TURNO
§
attiva il
laboratorio di emodinamica
INFERMIERE
LEADER
§
provvede
al passaggio delle informazioni all’infermiere dell’emodinamica e
trasporto del paziente al laboratorio di emodinamica.
DOPO
LA PROCEDURA
INTERVENTI:
§
Il
paziente trasferito in T.I: viene preso in carico dall’infermiere di
riferimento che riceve informazioni dal collega del laboratorio di emodinamica:
-
terapia effettuata e quella in corso
-
tipo di tecnica usata cioè PTCA con stent o senza
-
eventuali complicanze durante la procedura
-IRA
trattato ecc.
§
Esecuzione
terapia medica prescritta come ad esempio carico di farmaco antiaggregante
piastrinico; di solito usato come prevenzione delle ristesosi precoci.
§
Programmare
l’esecuzione dei marcatori cardiaci seriati: primo campione tra la 6- 10 ora
dall’arrivo in T.I. e secondo campione tra la 16-24 ora dall’arrivo in T:I
CRITICITA’
CLINICHE:
§
individuazione
precoce delle complicanze legate alla patologia di base e alla procedura:
Cardiache
Neurologiche
Legate
all’accesso arterioso
Nefrologiche
Correlate
alla terapia anticoagulante e antiaggregante
Legate
ad una embolizzazione di trombi o di cristalli di colesterolo con conseguenze a
livello degli organi, ad esempio disfunzioni renali.
Complicanze
cardiache:
Trombosi
acuta e subacuta intrastent
Dissecazione
della coronaria trattata
Edema
polmonare da sovraccarico di liquidi
Spasmo
coronarico
Tamponamento
cardiaco
INTERVENTI:
§
Osservazione
clinica del paziente: dolore anginoso, dispnea ecc.
§
Controllo
dei parametri vitali
§
Esecuzione
ECG subito dopo la procedura e ad ogni segno o sintomo indicatore di complicanze
Complicanze
neurologiche:
embolia
gassosa
embolia
colesterinica da placca aortica
INTERVENTI:
§
Osservazione
dello stato di coscienza: ben orientato; vigile; obnubilato ecc.
§
Agitazione
psicomotoria( sintomo iniziale di ipossia)
§
Deficit
sensoriale/motorio: tatto; linguaggio ecc.
§
Predisporre
se necessario per una eventuale consulenza neurologica
Complicanze
correlate all’accesso arterioso:
ematomi
pseudoaneurisma
fistola
artero-venosa
dissecazione
dell’arteria femorale
possibili
ischemie acute dell’arto a valle della puntura
INTERVENTI:
§
Rilevare
precocemente la formazione di ematomi attraverso:
§
palpazione
locale
§
valutazione
del dolore locale
§
preparazione
uso strumentale se sussiste il sospetto (eco-doppler)
Alla
rimozione dell’accesso arterioso:
§
osservazione
clinica del grado di perfusione dell’arto (polsi periferici; dolore e
parestesie; calore e temperatura della cute)
§
presenza
di soffusione emorragica
§
presenza
di soffi femorali
La
chiusura dell’accesso arterioso femorale è eseguita:
§
per
compressione con consecutivo posizionamento di tampone compressivo nelle
successive 24 ore
§
mediante
device (angioseal)
Il
valore di riferimento dell’ACT per la rimozione dell’accesso arterioso è
inferiore a 150 sec. da eseguire dopo 2-3 ore dalla fine della procedura .
Complicanza
nefrologiche:
IMPORTANZA
DI UNA ATTENTA ANAMNESI PER LE PATOLOGIE FAVORENTI LA NEFROPATIA
·
Si ritiene
che una ridotta funzionalità renale (CREA 1.8 mg/dl) aumenti il rischio di
danno nefrotossico da MDC di oltre 20 volte rispetto ad un individuo con
funzionalità renale nella norma (STUDIO Gruber e associati).
·
L’ipovolemia,
qualsiasi sia la causa, provoca un ipoperfusione renale che aumenta il rischio
di NMC.
·
Gli
ipertesi gravi sono più a rischio di NMC in quanto i vasi renali sono già
soggetti a vasospasmo nell’ambito del meccanismo dell’autoregolazione.
·
L’associazione
di una funzionalità renale già compromessa e diabete è in assoluto quella da
considerarsi a maggior rischio.
·
I
MDC sono notoriamente nefrotossici. I principali fattori di rischio legati al
mezzo di contrasto comprendono la dose, l’osmolarità e quindi il tipo di MDC
usato
.
INTERVENTI:
§
Ottimale
idratazione:
A
tutti i pazienti con CREATINEMIA superiore a 1.4 mg % (1.2 mg% nei diabetici)
infondere soluzione isotonica ( sol. Salina 0.9% ) , se non vi sono
controindicazioni, prima e dopo il cateterismo. L’idratazione con soluzione
isotonica riduce l’osmolarità degli ioni Na+.
Complicanze
correlate alla terapia anticoagulante. e antiaggregante:
Oltre
al bolo di Eparina ( di solito 5000 U) praticato durante la procedura, i
pazienti sottoposti a PTCA iniziano, in Unità Coronaria o in sala di
emodinamica in base ad una valutazione dell’emodinamista, l’infusione di
inibitori delle glicoproteine IIb/IIIa che poi proseguiranno per ulteriori 12
ore salvo diverse disposizioni. Si
possono verificare:
§
emorragie
maggiori (cerebrali)
§
emorragie
minori (epistassi)
§
piastrinopenia:
è significativa se i valori di PLT sono inferiori a 100.000; è critica se i
valori sono inferiori a 50.000.
INTERVENTI:
§
Controllo
dei parametri ematochimici della coagulazione
§
Controllo
dei segni clinici: ematoma in sede puntoria, petecchie, sanguinamenti gengivali
ecc.
CRITICITA’
RELAZIONALI:
§
Ansia
primaria, paura
che qualcosa non sia andata bene
INTERVENTI:
§
L’
infermiere deve porsi come punto di riferimento principale cui attingere
risposte e rassicurazioni su dubbi, paure e perplessità scaturite da quella
esperienza.
§
Coinvolgimento
attivo del paziente; invitarlo a segnalare tempestivamente la riacutizzazione
del dolore; a tale proposito l’infermiere deve saper discernere:
v
dolore
come sintomo di complicanza cliniche ( dolore da angina; dolore da ischemia
periferica o da compressione da ematoma );
v
dolore
legato a stanchezza, posture obbligate prolungate;
v
dolore
toracico residuo da stress coronario ( transitorio ).
PTCA
DI SALVATAGGIO O RESCUE
Viene
eseguita quando la terapia fibrinolitica è giudicata inefficace.
I
criteri indicativi di riperfusione inefficace secondo De Lemos et al. sono:
v
risoluzione
del segmento ST inferiore 50% a 90 minuti;
v
dolore
toracico persistente a farmaci.
Il
modello assistenziale infermieristico, naturalmente è valido quello appena
descritto.
CONCLUSIONI
La
riflessione sull’agire quotidiano, fa ripensare a: “ come in questa società
così tecnologica, in una cardiologia così avanzata, la parola di un uomo,
paziente o infermiere; lo sguardo riconoscente di un malato, siano e saranno al
di là del tempo INSOSTITUIBILI, concorrendo oggi come domani ad alimentare
quella professionalità tanto auspicata, fatta di competenze, di conoscenze e
tecnica, ma anche di pensieri, parole ed emozioni” (A. BONANSEA).
BIBLIOGRAFIA:
1.
Linee guide European Society of Cardiology
2.
Documento di
Consenso della Federazione Italiana di Cardiologia ANMCO/SIC 2002
3.
Atti del V
Congresso Nazionale Chianciano Terme, 11 – 13 aprile 2002
4.
Atti del
XXXIV Congresso Nazionale di Cardiologia dell’ANMCO 2003
5.
Manuale di ACLS – American Heart Association 2003
6.
Trombolisi
preospedaliera – Presentazione Dr G. Di Pasquale-
SITI
INTERNET:
1.
e/cardiologia
.it
2.
http://medlib.med.utah.edu/kw/ecg