osservazioni sul cambiamento di colore che
assumono particolari sostanze in presenza di
ambienti acidi o basici : indicatori chimici e misura di pH
una soluzione si definisce acida,neutra,basica
in funzione di un parametro detto pH
se pH varia da 0 a <7 si dice acida
se pH =7 si dice neutra
se pH varia da >7 a 14 si dice basica
certe sostanze poste in un soluzione modificano il loro colore
in funzione del grado di acidità della soluzione,cioè del pH:
tali sostanze si definiscono Indicatori chimici
osservazioni per verificare entro quali valori di pH alcuni indicatori
modificano il loro colore (viraggio dell’indicatore)
materiale
-soluzioni acide e basiche con pH noto
-provette per analisi
-serie di 5 indicatori chimici (cartine indicatrici o soluzioni)
-tornasole,metil arancio,fenolftaleina,blu timolo,giallo alizarina
fase operativa
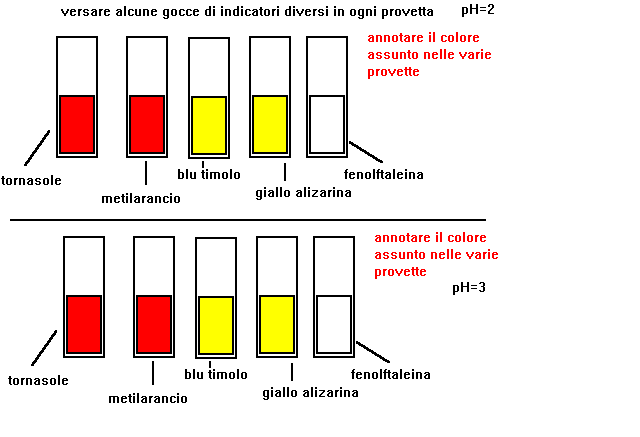
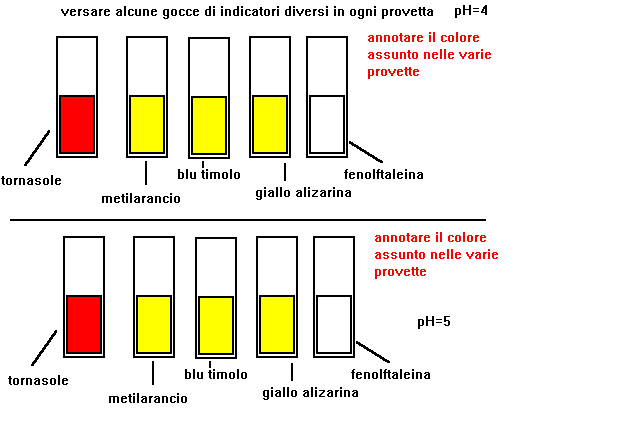
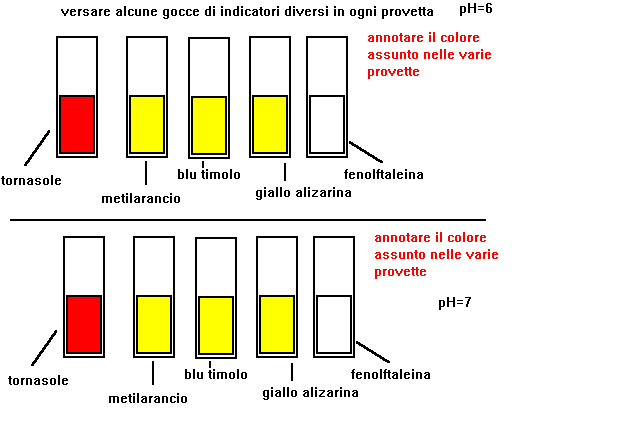
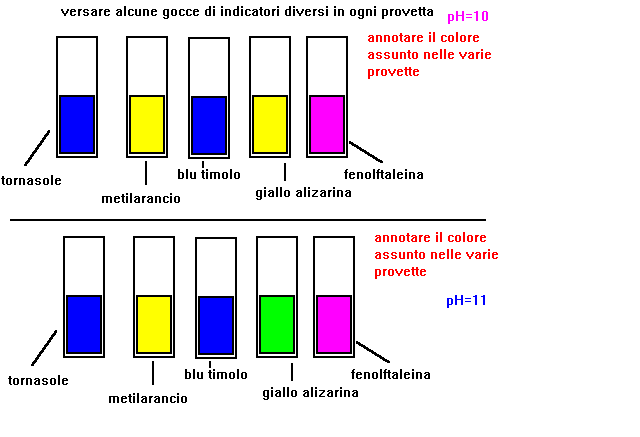
1-prendere 5 provette e versare in ciascuna circa 5 cc.di soluzione con pH=1
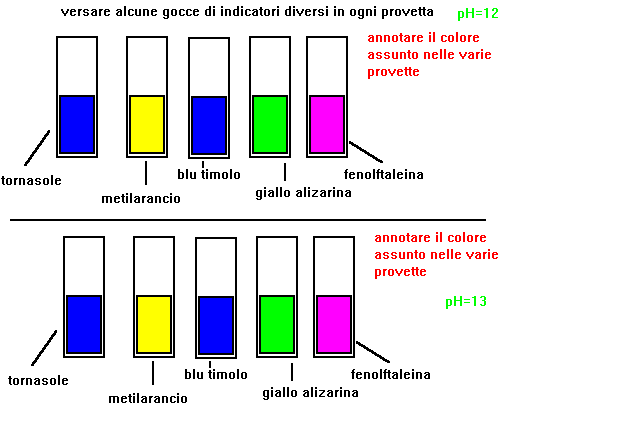
2-versare alcune gocce di un indicatore diverso in ogni provetta
3-prendere nota del colore assunto dalla soluzione
4-ripetere le operazioni precedenti (da 1 a 3) con soluzione a pH
variabile:pH=2,3,4,5,6,7,8,9,10,11,12,13,14
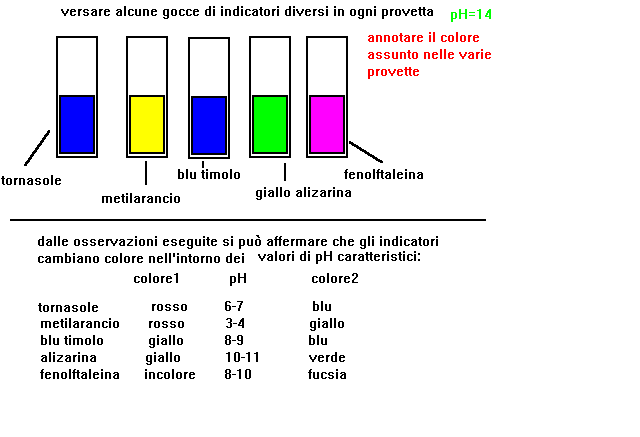
5-indicare per quali valori di pH ogni indicatore cambia di colore
6-si verifica che per ogni indicatore esistono due campi di valori
di pH entro i quali il colore rimane costante,e un piccolo campo
compreso tra i due precedenti,entro il quale avviene il viraggio
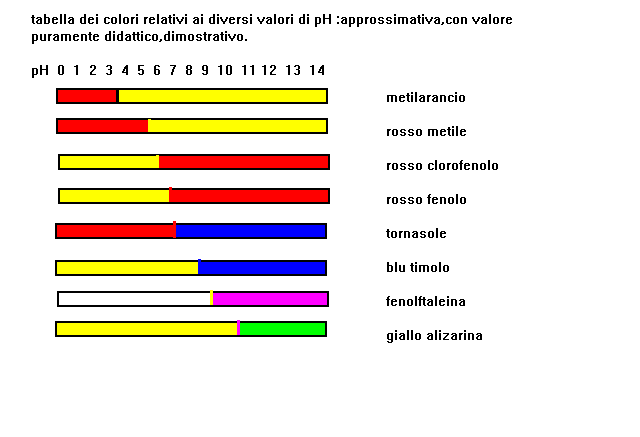
7-sfruttando tale comportamento si potranno analizzare soluzioni
con pH incognito e determinarlo in via approssimativa.